
苏州纳米所氧化石墨烯载药系统研究取得系列进展
作为新型二维纳米材料石墨烯的重要衍生物,氧化石墨烯(GO)在生物医学领域的应用研究引起了人们的广泛兴趣,已经成为纳米生物医学,尤其是纳米载药的研究热点之一。GO作为纳米载药系统的主要优点包括:(1)具有超大的比表面,从而可以实现超高载药率;(2)具有很强的靶向性,容易在肿瘤部位富集;(3)功能化GO在生理条件下具有良好的生物相容性和稳定性。
最近中国科学院苏州纳米技术与纳米仿生研究所张智军研究员课题组在氧化石墨烯载药系统构建研究方面取得系列进展。首先该课题组利用聚乙二醇(PEG)修饰GO作为蛋白递送载体用于细胞功能调控。蛋白药物生物活性好、毒性低,但易被生物体内存在的蛋白酶所降解,而且不能有效的递送到细胞内,导致其生物利用度大大降低,从而严重影响了蛋白药物的疗效。该课题组研究发现,GO不仅可以高效的负载蛋白,还可以有效的保护其不被酶水解。更重要的是,GO可以递送不同的功能性蛋白进入细胞,实现其对细胞的生理功能的有效调控(ACS Appl. Mater. Interfaces, 2012, 4, 6317-6323)。在此基础上,该课题组与苏州大学附属第二医院兰青教授团队合作,将转铁蛋白共价修饰在PEG化的GO表面,使药物递送体系可以穿过血脑屏障,进而将抗癌药物阿霉素(DOX)靶向递送至脑胶质瘤部位(图1)。体内试验表明,该递送系统可以靶向递送DOX至胶质瘤部位,并有效抑制肿瘤生长,显著延长荷瘤大鼠存活时间(ACS Appl. Mater. Interfaces, 2013, 5, 6909-6914)。
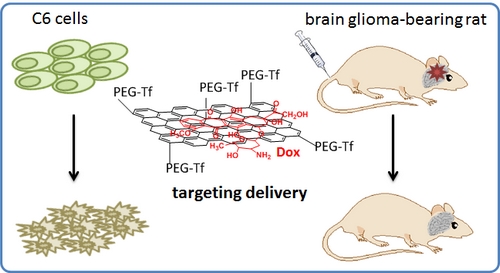
图1. 转铁蛋白修饰的氧化石墨烯用于脑胶质瘤靶向药物递送示意图
临床上联合给药能够减少药物的多药耐药性、增强药物的协同抗肿瘤效果。该课题组曾经开展了氧化石墨烯联合递送抗癌药物DOX和喜树碱、DOX与肿瘤抗凋亡蛋白Bcl2靶向的siRNA的工作(Small, 2010, 6, 537-544; Small, 2011, 7, 460-464)。最近他们发现,通过PEG修饰氧化石墨烯有效负载难溶性的蛋白激酶抑制剂BEZ235,与肿瘤坏死因子TNF-α联合作用后,对PIK3CA突变细胞系HCT 116能引起其G1期阻滞和肿瘤细胞细胞凋亡。他们还进一步研究了联合载药治疗肿瘤机制,发现细胞凋亡主要是由于联合用药引起JNK磷酸化水平增加,及caspase-8的激活,进而激活caspase-9以及caspase-3(图2)(Journal of Materials Chemistry B, 2013, DOI:10.1039/C3TB
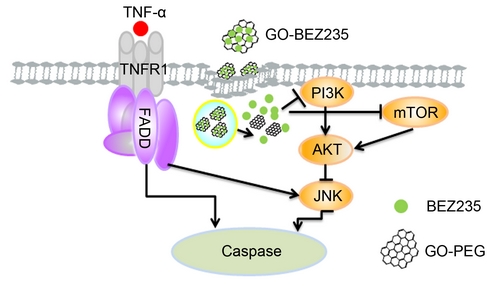
图2. GO-BEZ235联合TNF-α引起HCT 116细胞凋亡信号通路示意图
此外,该课题组与东南大学

图3. 张智军课题组研究成果被选为J. Mater. Chem. B封面文章。
阐明GO进入细胞的途径及机制以及细胞内药物从GO表面的释放行为对于研制新型高效氧化石墨烯载药系统具有重要意义。该课题组与厦门大学固体表面物理化学国家重点实验室
该课题组在氧化石墨烯载药系统的系列研究成果受到国际同行的关注,最近该课题组受邀在国际学术期刊Theranostics上发表综述文章“Biomedical Applications of Graphene”(Theranostics, 2012, 3(2), 283-294)。
上述工作得到国家自然科学基金、科技部、中科院以及江苏省自然科学基金等经费支持。
附件下载:

